Kompetensi Dasar :
Pengetahuan
3.8. Menghubungkan konsep partikel materi (atom, ion, molekul), struktur zat sederhana dengan sifat bahan yang digunakan dalam kehidupan sehari-hari, serta dampak penggunaannya terhadap kesehatan manusia.
Keterampilan
4.8. Menyajikan hasil penyelidikan tentang sifat dan pemanfaatan bahan dalam kehidupan sehari - hari.
Tujuan Pembelajaran :
Setelah mengikuti proses pembelajaran daring, peserta didik dapat :
1. Mengidentifikasi penyusun atom dengan benar.
2. Mendeskripsikan perkembangan teori atom dengan benar.
3. Menentukan nomor atom dan nomor massa suatu atom dengan benar.
4. Menganalisis perbedaan atom, molekul, unsur dan senyawa dengan benar.
Assalamualaikum Wr. Wb
Anak-anak, sebelum kita belajar IPA hari ini, jangan lupa untuk berdoa terlebih dahulu. Dengan doa dan upaya kalian yang sungguh-sungguh, Pak Arief yakin kalian akan mampu menguasai materi hari ini. Berikut Peta Konsep materi yang akan kita pelajari.
PETA KONSEP
APERSEPSI
Sebelum melanjutkan membaca ringkasan materi, silakan disimak dulu video berikut ini untuk memberikan gambaran mengenai materi yang akan kita pelajari.
RINGKASAN MATERI
Partikel adalah bagian terkecil dari suatu materi yang masih mempunyai sifat materi itu sendiri. Partikel dapat berbentuk atom, molekul, dan ion. Atom adalah bagian terkecil dari suatu unsur yang masih memiliki sifat unsur tersebut. Atom-atom dapat berikatan satu sama lain membentuk molekul. Molekul merupakan gabungan antara dua atau lebih atom-atom melalui ikatan kimia tertentu. Molekul dapat tersusun sedemikian rupa sehingga menjadi suatu struktur tertentu, misalnya rambut, tersusun dari molekul-molekul yang mengandung unsur karbon (C), hidrogen (H), nitrogen (N), dan sulfur (S). Sedangkan tulang, mengandung kalsium (Ca), fosfor (P), dan oksigen (O).
A. Atom dan Penyusunnya
1. Partikel Sub Atom
- Partikel penyusun benda mati dan makhluk hidup yang terkecil adalah atom.
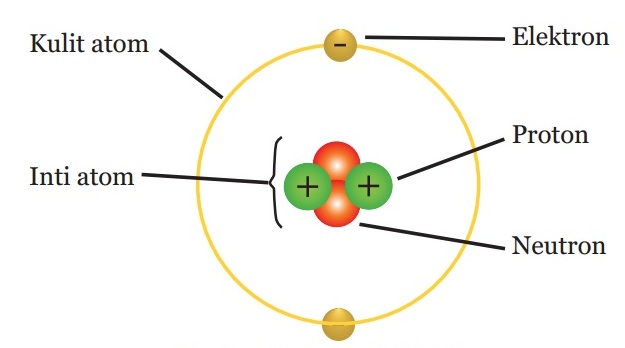
- Atom tersusun atas partikel-partikel penyusun atom atau partikel subatom yaitu neutron (n), proton (p), dan elektron (e).
- Neutron merupakan partikel subatom yang tidak mempunyai muatan/netral.
- Proton merupakan partikel subatom yang mempunyai muatan positif (+).
- Elektron merupakan partikel subatom yang mempunyai muatan negatif (-).
- Neutron dan proton membentuk inti atom. Elektron menempati kulit-kulit atom yang ada di sekitar inti atom.
- Elektron-elektron tersebut bergerak mengelilingi inti dengan kecepatan tinggi membentuk awan elektron.
- Bila jumlah elektron dan jumlah proton dalam suatu atom tidak sama, atom tersebut akan bermuatan atau menjadi ion. Proses pembentukan ion disebut ionisasi.
2. Perkembangan Teori Atom
Berikut ini merupakan perkembangan teori atom.a. Teori Atom Dalton- Atom sebagai bola pejal dan merupakan bagian terkecil yang tidak dapat dibagi lagi.
- Setiap unsur terdiri atas atom-atom yang identik satu sama lain.
- Atom-atom dari unsur berbeda mempunyai atom berbeda.
- Atom-atom dapat bergabung dengan perbandingan tertentu membentuk senyawa.
- Atom merupakan bola bermuatan positif dan di tempat-tempat tertentu terdapat elektron-elektron yang bermuatan negatif seperti kismis dalam roti.
- Atom sebagai bola yang di tengah-tengahnya terdapat inti atom yang merupakan pusat muatan positif dan pusat massa.
- Sedangkan elektron-elektron berputar mengelilingi inti.
- Atom terdiri terdiri atas inti yang menjadi pusat massa atom dan pusat muatan positif.
- Sedangkan elektron bergerak di sekeliling inti pada lintasan tertentu (orbit) yang disebut kulit-kulit atom.
- Selama elektron mengelilingi inti, elektron tidak memancarkan energi.
- Atom tersusun atas partikel sub atom yaitu neutron (n), proton (p), dan elektron (e).
- Neutron dan proton menjadi satu membentuk inti yang padat disebut nukleus atau inti atom.
- Elektron bergerak disekeliling inti hampir dalam kecepatan cahaya membentuk awan elektron.
- Atom-atom dari unsur yang berbeda memiliki jumlah partikel subatom yang berbeda.
- Setiap atom memiliki nomor atom dan nomor massa.
- Nomor atom menunjukkan jumlah proton, sedangkan nomor massa menunjukkan jumlah proton dan neutron.
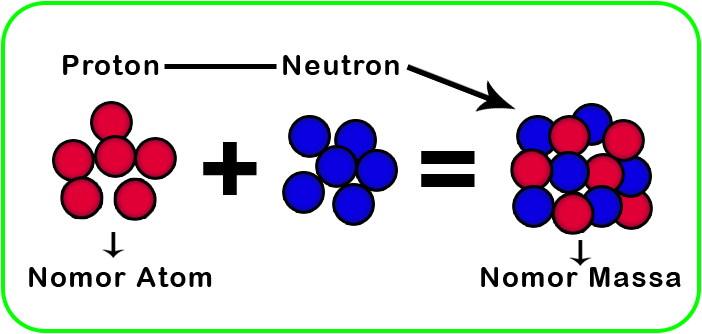
Nomor atom = Jumlah proton (p) = Jumlah elektron (e)
Nomor massa = Jumlah proton (p) + Jumlah neutron (n)
4. Isotop, Isobar dan Isoton
- Isotop adalah atom-atom yang memiliki nomor atom sama tetapi berbeda nomor massanya. Contohnya:
- Isobar adalah atom yang mempunyai nomor atom berbeda tetapi memiliki nomor massa yang sama. Contohnya:
- Isoton adalah atom yang mempunyai nomor atom dan nomor massa berbeda tetapi memiliki jumlah neutron yang sama. Contohnya:
B. Perbedaan Atom, Molekul, Unsur dan Senyawa
- Atom merupakan partikel penyusun materi yang terkecil.
- Molekul merupakan gabungan dari dua atom atau lebih yang berasal dari unsur yang sama atau berbeda dan saling berikatan.
- Apabila atomnya berasal dari unsur yang sama, maka molekul tersebut dinamakan molekul unsur.
- Jika satu molekul tersusun atas dua atau lebih atom dari unsur yang berbeda, maka disebut molekul senyawa.
- Unsur merupakan suatu zat tunggal yang tidak dapat disederhanakan lagi dengan menggunakan reaksi kimia biasa.
- Apabila suatu unsur hanya terdiri dari satu atom saja, maka dinamakan unsur tunggal.
- Senyawa merupakan gabungan dari beberapa unsur.
Perhatikan ilustrasi berikut !
Dari gambar ilustrasi di atas, sudah ada yang bisa membedakan atom, molekul, unsur dan senyawa ? Jika masih bingung, coba perhatikan ilustrasi berikut !
Pada gambar di atas:
- Terdapat satu jenis unsur, yaitu karbon (C).
- Terdapat satu buah atom, yaitu satu atom karbon (C).
- Disebut unsur tunggal karena terdiri dari satu atom saja.
- Terdapat satu jenis unsur, yaitu oksigen (O).
- Terdapat dua buah atom, yaitu dua atom hidrogen (H) dan satu atom oksigen (O).
- Disebut molekul unsur karena terdiri dari dua atom yang berasal dari unsur yang sama.
Pada gambar di atas:
- Terdapat dua jenis unsur, yaitu hidrogen (H) dan oksigen (O).
- Terdapat tiga buah atom, yaitu dua atom hidrogen (H) dan satu atom oksigen (O).
- Bisa disebut senyawa karena terdiri dari dua unsur yang berbeda.
- Bisa disebut molekul senyawa karena terdiri dari dua atom atau lebih yang berasal dari unsur yang berbeda.
REFERENSI
- Video referensi : Beberapa video referensi terkait materi bisa dilihat dengan cara klik pada gambar.
LATIHAN SOAL
Setelah mempelajari materi ini, sekarang ayo dicoba untuk mengerjakan latihan soalnya.
Catatan :
Format Penulisan Identitas untuk mengerjakan latihan soal :
"Nama Lengkap/Kelas"
Contoh : Adellia Larasati/9A
~ Tetap Semangat Belajar IPA #dirumahaja ~








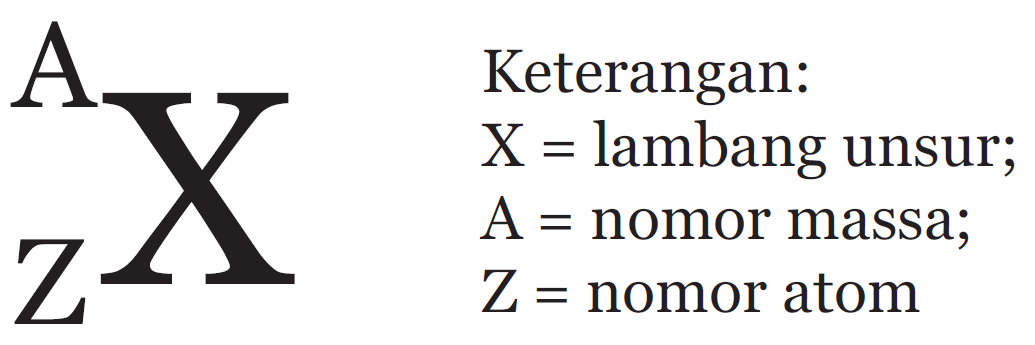
















Tidak ada komentar:
Posting Komentar